【中3】金属イオンへのなりやすさ
単元:金属イオンへのなりやすさ
問題
金属イオンへのなりやすさを調べる実験をしました。
まず、3種類の水溶液を試験管の中に入れたものをそれぞれ3本ずつ用意し、マグネシウム、亜鉛、銅の3種類の金属板をそれぞれ加え、反応を調べる実験をしました。表は、その結果を示したものです。
後の問いに答えなさい。
| マグネシウム板 | 亜鉛板 | 銅板 | |
| 硫酸マグネシウム水溶液 | 反応なし | 反応なし | 反応なし |
| 硫酸亜鉛水溶液 | A(黒色の物質が付着) | 反応なし | 反応なし |
| 硫酸銅水溶液 | B(赤色の物質が付着) | C(赤色の物質が付着) | 反応なし |
(1)B,Cの赤色の物質名を答えなさい。
(2)表の結果から、イオンのなりやすさの順番を答えなさい。
(3)Aで起きた反応について
①水中に溶けだした板名とイオン名を答えなさい。
②Aの物質ができる反応をイオン式で表しなさい。

まず問題(1)から考えていきましょう。
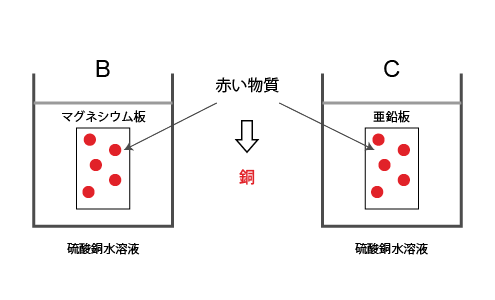
表中のBではマグネシウム板に,Cでは亜鉛版にそれぞれ赤色の物質が付着しました。
赤い物質に関係しているのは両方とも硫酸銅水溶液に含まれている銅だけですので、この赤い物質は銅であると考えられます。
表中のBではマグネシウム板に,Cでは亜鉛版にそれぞれ赤色の物質が付着しました。
赤い物質に関係しているのは両方とも硫酸銅水溶液に含まれている銅だけですので、この赤い物質は銅であると考えられます。


なぜBとCには金属板に銅が付着したのでしょうか。

良い質問ですね。ではBを例に説明します。Bでは硫酸銅水溶液にマグネシウム板を入れました。
すると下のような反応が起こります。まずマグネシウム原子が電子を2個放出してマグネシウムイオンとなり、水溶液中に溶け出します。すると放出された電子2個を、硫酸銅水溶液に含まれる銅イオンが受け取り,銅原子となってマグネシウム板に付着します。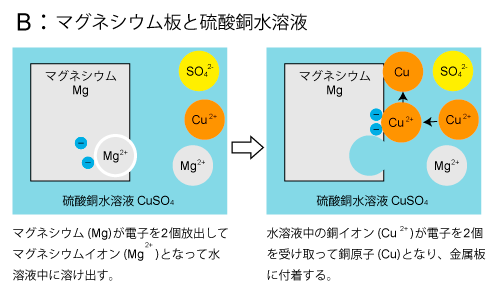
すると下のような反応が起こります。まずマグネシウム原子が電子を2個放出してマグネシウムイオンとなり、水溶液中に溶け出します。すると放出された電子2個を、硫酸銅水溶液に含まれる銅イオンが受け取り,銅原子となってマグネシウム板に付着します。


なるほど!でも表を見ると変化がなかったものもあります。これはなぜでしょうか。

これは金属の陽イオンへのなりやすさに関係しています。Bでは、金属板のマグネシウムが硫酸銅水溶液に含まれる銅よりも陽イオンになりやすいため、マグネシウムイオンとなって水溶液中に溶け出しました。
反対に金属板の金属が水溶液中の金属よりも陽イオンになりにくい場合は,金属板は溶け出さないため、Bのような反応は起こりません。このような,金属の陽イオンへのなりやすさをイオン化傾向といいます。
反対に金属板の金属が水溶液中の金属よりも陽イオンになりにくい場合は,金属板は溶け出さないため、Bのような反応は起こりません。このような,金属の陽イオンへのなりやすさをイオン化傾向といいます。

なるほど!そうすると、この実験から銅・マグネシウム・亜鉛の陽イオンへのなりやすさの順番がわかります。
マグネシウム板は硫酸亜鉛水溶液と硫酸銅水溶液のどちらにいれても変化があったため、マグネシウムが1番陽イオンになりやすいと言えますね。反対に銅板はどの水溶液に入れても変化がなかったため、銅は1番陽イオンになりにくいと言えます。
よって(2)の答えは、 です。
です。
マグネシウム板は硫酸亜鉛水溶液と硫酸銅水溶液のどちらにいれても変化があったため、マグネシウムが1番陽イオンになりやすいと言えますね。反対に銅板はどの水溶液に入れても変化がなかったため、銅は1番陽イオンになりにくいと言えます。
よって(2)の答えは、
 です。
です。

正解です!では以上のことを踏まえて、問題(3)も考えてみましょう。

えーと、これまでの話からわかることは、
マグネシウム原子は電子を2個放出してマグネシウムイオンとなり,硫酸亜鉛水溶液中に溶け出す。
放出された電子は、硫酸亜鉛水溶液中の亜鉛イオンが受け取り,亜鉛原子となって、マグネシウム板に付着した。
このことから,マグネシウムの方が亜鉛よりも陽イオンになりやすいことが分かります。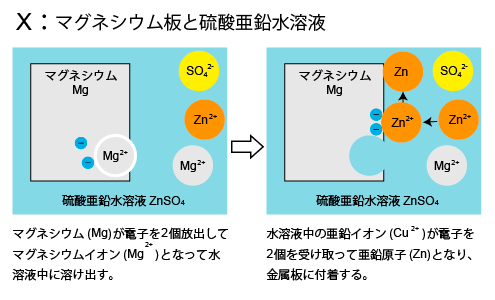 よって水中に溶けだした板名はマグネシウムです。
よって水中に溶けだした板名はマグネシウムです。
イオン名はマグネシウムイオンです。
マグネシウム原子は電子を2個放出してマグネシウムイオンとなり,硫酸亜鉛水溶液中に溶け出す。
放出された電子は、硫酸亜鉛水溶液中の亜鉛イオンが受け取り,亜鉛原子となって、マグネシウム板に付着した。
このことから,マグネシウムの方が亜鉛よりも陽イオンになりやすいことが分かります。
 よって水中に溶けだした板名はマグネシウムです。
よって水中に溶けだした板名はマグネシウムです。イオン名はマグネシウムイオンです。

正解です!よく出来ました!
次に、Aの物質ができる反応をイオン式で考えてみましょう。
まず、マグネシウムは溶けだしたので電子を2個失ってマグネシウムイオンになるので
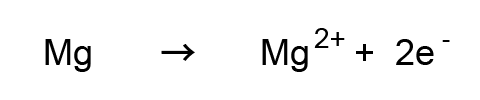 となります。これを参考に考えてみましょう。
となります。これを参考に考えてみましょう。
次に、Aの物質ができる反応をイオン式で考えてみましょう。
まず、マグネシウムは溶けだしたので電子を2個失ってマグネシウムイオンになるので
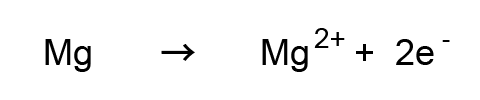 となります。これを参考に考えてみましょう。
となります。これを参考に考えてみましょう。

Aの反応では付着した物質は亜鉛なので、亜鉛イオンが電子を2個受け取って亜鉛になる反応を考えればいいから
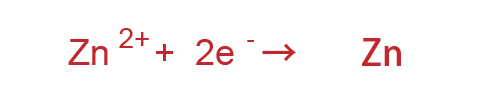
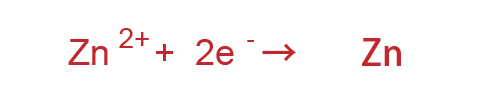

正解です!
テストではイオン式を書く問題も出題されるのでしっかり覚えておきましょう。
テストではイオン式を書く問題も出題されるのでしっかり覚えておきましょう。
ITTO長野の中学生理科プラン
学習の状況と志望校をお伺いしながらプランはご案内いたします。詳しくは各教室まで。例えばこんなプランで









